 Научные и курсовые работы |
Главная
Исторические личности
Военная кафедра
Ботаника и сельское хозяйство
Бухгалтерский учет и аудит
Валютные отношения
Ветеринария
География
Геодезия
Геология
Геополитика
Государство и право
Гражданское право и процесс
Естествознанию
Журналистика
Зарубежная литература
Зоология
Инвестиции
Информатика
История техники
Кибернетика
Коммуникация и связь
Косметология
Кредитование
Криминалистика
Криминология
Кулинария
Культурология
Логика
Логистика
Маркетинг
Наука и техника Карта сайта
Курсовая работа: Кондуктометрический метод анализа и его использование в анализе объектов окружающей природной среды
Курсовая работа: Кондуктометрический метод анализа и его использование в анализе объектов окружающей природной среды
Кондуктометрический метод анализа и его использование в анализе объектов окружающей природной среды
Введение
К началу XXI века стало ясно, что электрохимический анализ, как и сама аналитическая химия, вышел за пределы своего классического содержания. Если раньше методология электрохимического анализа по большей части развивалась на основе изучения объектов неорганической природы, то сейчас электрохимический анализ устойчиво «дрейфует» в сторону решения проблем экологии, анализа биологических и медицинских объектов, в которых органическое вещество встречается все чаще и чаще. В решении задач собственно электрохимического анализа актуальным становится конструирование модифицированных электродов, которые дают специфический отклик благодаря иммобилизации на электроде органических молекул или их фрагментов, например ДНК или ее олигомеров. Повышение интереса к анализу объектов органической природы предопределено тем, что число последних на несколько порядков превышает число ионов металлов и их соединений. При этом все шире используется разнообразие электродных процессов, более сложных форм электрического воздействия на изучаемый объект и преобразования аналитического сигнала, в том числе на основе достижений математики, информатики и электронной техники. Очевидно, что необходимый уровень знаний в этой сфере является непременным условием успешной деятельности специалистов в области электрохимического анализа, способных творчески применять и развивать указанные методы. Одним из распространенных методов является кондуктометрия. Кондуктометрия используется в работе анализаторов детергентов в сточных водах, при определении концентраций синтетических удобрений в оросительных системах, при оценке качества питьевой воды. В дополнение к прямой кондуктометрии для определения некоторых видов загрязнителей могут быть использованы косвенные методы, в которых определяемые вещества взаимодействуют перед измерением со специально подобранными реагентами и регистрируемое изменение электропроводности вызывается только присутствием соответствующих продуктов реакции. Кроме классических вариантов кондуктометрии применяют и ее высокочастотный вариант (осциллометрию), в котором индикаторная электродная система реализуется в кондуктометрических анализаторах непрерывного действия.
1. Теоретические основы кондуктометрического метода анализа
Кондуктометрические методы анализа основаны на измерении электропроводности исследуемых растворов. Существует несколько методов кондуктометрического анализа:
· прямая кондуктометрия – метод, позволяющий непосредственно определять концентрацию электролита путем измерения электропроводности раствора с известным качественным составом;
· кондуктометрическое титрование метод анализа, основанный на определении содержания вещества по излому кривой титрования. Кривую строят по измерениям удельной электропроводности анализируемого раствора, меняющейся в результате химических реакций в процессе титрования;
· хронокондуктометрическое титрование – основано на определении содержания вещества по затраченному на титрование времени, автоматически фиксируемого на диаграммной ленте регистратора кривой титрования.
Кондуктометрия
Кондуктометрия относится к наиболее распространенным методам исследования растворов и жидких систем вообще.
· проводящими принято условно с χ ~10-7 Ом-1·см-1 и выше;
· умеренно проводящими с χ: 10-7 – 10-11 Ом-1 ·м-1;
· непроводящими – χ ниже 10-11 Ом-1 ·м-1.
Данная классификация условна.
В ФХА принято пользоваться диаграммами «удельная электропроводность χ – состав». Поскольку электропроводность относится к заведомо не аддитивным свойствам, способ выражения концентрации при этом может быть произвольным, однако для наглядности чаще всего выбирают мольные доли. Диаграммы «молекулярная электропроводность λ – состав» используется реже.
Электрическое сопротивление
Основной константой, характеризующей электрические свойства вещества, является удельное электрическое сопротивление, зависящее от природы вещества и от температуры.
Согласно закону Ома удельное электрическое сопротивление (ρ) [Ом·м]:
![]() ,
,
где R – электрическое сопротивление, ом; S – площадь поперечного сечения, м2; l – длина, м.
Температурная зависимость электрического сопротивления металлов подчиняется закону:
ρt = ρ0 (1+αt),
где α – температурный коэффициент.
Электрическая проводимость обусловлена движением заряженных частиц и зависит от количества носителей заряда и их подвижности.
Для разбавленных твердых растворов, их удельное электрическое сопротивление по правилу Маттиссена представлено из двух слагаемых:
ρ = ρ(t) + ρ(x),
где ρ(t) – электрическое сопротивление чистого металла, зависящее от температуры метала; ρ(x) остаточное электрическое сопротивление, не зависящее от температуры и определяется типом примеси и ее концентрацией.
Эта формула применима при содержании примеси до 1 ат.% Согласно правилу Линде, добавочное электрическое сопротивление, вызываемое содержанием примеси 1 ат.%, пропорционально квадрату разности валентностей чистого металла и примеси (∆z):
∆ρ(x) = a + b(∆z)2,
где a, b – величины, определяющие свойства металла – растворителя.
Правило Маттиссена достаточно хорошо выполняется для большинства разбавленных металлических расплавов, правилу Линде многие расплавы не подчиняются.
Механизм электрической проводимости в металлических расплавах и твердых металлах принципиально не различается.
Переход металла из твердого в жидкое состояние сопровождается некоторым изменением электрических свойств: при плавлении удельное электросопротивление большинства металлов увеличивается в 1,5÷2 раза. Для некоторых металлов (Bi, Sb, As) характерно аномальное поведение: при плавлении их удельное электросопротивление уменьшается.
Электрическая проводимость оксидных расплавов близка к электропроводимости типичных электролитов (галлогениды щелочных металлов) и зависит от состава шлака и температуры. Это является одним из доказательств ионной теории строения шлаковых расплавов.
Их ионная структура определяет преимущественно ионную проводимость в расплавленном состоянии. Электропроводимость определяется, в первую очередь, размерами катионов и анионов и силами взаимодействия между ними.
Повышение температуры увеличивает электропроводимость оксидных расплавов. При переходе из твердого состояния в жидкое электропроводимость резко возрастает.
Уравнение Я.И. Френкеля характеризует температурную зависимость электропроводимости ионных кристаллов:
![]()
Уравнение применимо и для оксидных расплавов, в которых перенос тока осуществляется только катионами (которые много меньше по размеру, чем анионы), т.е. если радиусы анионов велики по сравнению с катионами, и анионы остаются почти неподвижными в электрическом поле.
При соблюдении уравнения Я.И. Френкеля
экспертные данные укладываются в прямолинейную зависимость ![]() . Отклонения свидетельствуют
о структурных изменениях, которые могут быть связаны с разложением комплексных
анионов на простые.
. Отклонения свидетельствуют
о структурных изменениях, которые могут быть связаны с разложением комплексных
анионов на простые.
![]() .
.
Контактные методы измерения электрической проводимости расплавов
В основе лежит закон Ома: на фиксированном участке проводника из жидкого металла, имеющего длину l и площадь поперечного сечения S, определяется электросопротивление Rχ.
Из соотношения ![]() устанавливают значения
удельной электропроводимости металла.
устанавливают значения
удельной электропроводимости металла.
Для определения электросопротивления проводника применяют следующие электрические измерительные схемы:
·
схема вольтметра-амперметра, в
которой при помощи вольтметра измеряют падение напряжения на концах проводника
Vx, а амперметром – силу тока I. В этом случае значение Rx
определяют по закону Ома: ![]() . Точность метода невысока (≤
1%) и определяется классом точности приборов.
. Точность метода невысока (≤
1%) и определяется классом точности приборов.
·
Компенсационный метод: в цепь
включают эталонное сопротивление Rэ и с помощью потенциометра
измеряют падение напряжения на проводнике Vx и эталоне Vэ.
Расчет по формуле: ![]() более точный метод.
более точный метод.
· С использованием моста Уитстона или двойного моста Томсона. Точность 0,2–0,3%, но необходимо учитывать контактные сопротивления и сопротивление проводов.
Определение электропроводимости расплавов связано с техническими трудностями: контакт расплава с электродами, подбор материалов.
Конструкции измерительных ячеек с различным расположением калиброванного канала, в котором проводник из жидкого металла, электроды токовые и потенциальные.
Для расчета удельного электрического сопротивления (или электрической проводимости) по измеренному (методом моста или методом вольтметра-амперметра) значению электрического сопротивления расплава необходимо знать константу ячейки. Градуировку ячейки обычно производят водным раствором (при комнатной температуре) или расплавом NaCl или KCl (при 700–900 °С).
Значение константы ячейки определяют по формуле:
![]() ,
,
где r – сопротивление проводящих проводов и электродов при соответствующих температурах опыта; Rx измеряемое сопротивление.
Одним из способов определения r является предварительное определение.
Чаще используют другой метод, заключающийся в измерении электросопротивления при двух последовательных погружениях электродов на различную глубину. Этот способ позволяет исключить поправку на сопротивление проводов (r), т. к. расчет удельного электрического сопротивления ведут по разности измеренных сопротивлений:
![]() ,
,
где К1 и К2 константы ячейки при двух последовательных погружениях электродов.
Конструкция установки разработанной Б.М. Лепинских и О.А. Есиным (УПИ) с мостовой схемой измерения и ячейкой типа электрод-электрод.
Регулирование глубины погружения электродов производится вращением стержня (#), при этом происходит подъем или опускание тигля при неподвижных электродах.
Среднее значение константы ячейки устанавливают градуированием по 0,1 н раствору KCl. Этот метод используется для определения электрической проводимости двойных шлаковых систем. Схема моста позволяет измерять сопротивление расплавов с точностью до 0,01 ом. Относительная ошибка определения удельной электрической проводимости двойных шлаковых систем. Схема моста позволяет измерять сопротивление расплавов с точностью до 0,01 ом. Относительная ошибка определения удельной электрической проводимости достигает 11,8%.
Кондуктометрия располагает несколькими законами:
1. В очень разбавленных растворах (предельно разбавленных) эквивалентная электропроводность (λ0) является постоянной характеристикой раствора, не зависящей от изменения концентрации электролита. Говоря простым языком, это означает, что в разбавленных растворах электропроводность прямопропорциональна количеству заряженных частиц – ионов.
Для растворов сильных электролитов область предельного разбавления простирается до концентрации 0,0001н, а с небольшой погрешностью можно считать границей предельного разбавления концентрацию 0,001н.
Для расчетов в области больших концентраций существует формула Кольрауша, но ее нельзя использовать для прогноза, поскольку она носит явно эмпирический характер:
λ = λ0 + K C 1/2,
2. Предельная эквивалентная электропроводность раствора электролита равна сумме эквивалентных электропроводностей катиона и аниона.
3. Эквивалентные электропроводности подавляющего числа ионов близки друг к другу по величине. Анализ экспериментальных данных показывает, что при 18 0С для катионов λ0=0,0053 ± 0,0019 Ом-1 м2 г-экв-1 и для анионов λ0=0,0055 ± 0,0027 Ом-1 м2 г-экв-1. При 25 0С λ 0=0,0062 ± 0,0023 Ом-1 м2 г-экв-1 для катионов и λ0=0,0064 ± 0,0031 для анионов. Исключение составляют ионы H+, OH-, Fe(CN)63-, Fe(CN)64-, электропроводности которых аномально высоки:
| Ион |
Эквивалентная электропроводность, |
|
|
18 0С |
25 0С |
|
|
H+ |
0,0315 | 0,03497 |
|
1/3 Fe(CN)63- |
- | 0,01009 |
|
1/4 Fe(CN)64- |
- | 0,01105 |
|
OH- |
0,0174 | 0,01976 |
4. Температура анализируемого раствора оказывает существенное влияние на измеряемые величины удельной электропроводности. В настоящее время не существует способа удовлетворительного описания влияния температуры на электропроводность. Причина такого положения дел кроется в слишком большом влиянии индивидуальной природы растворенных веществ на температурный коэффициент. С уверенностью можно сказать только одно: при повышении температуры на один градус удельная электропроводность раствора в среднем увеличивается на 1–2,5%.
Прямые кондуктометрические измерения
Аналитическое использование кондуктометрии обладает характерными чертами, связанными с низкой селективностью кондуктометрического детектирования. В самом деле, близкие значения эквивалентных электропроводностей ионов не позволяют говорить о том, что какой-либо ион может целиком определять электропроводность всего раствора. Таким образом, измерения электропроводности может приносить реальную аналитическую пользу только в том случае, если соотношение ионов в анализируемой смеси неизменно от пробы к пробе. Это, так называемая, задача определения разбавления исходного раствора. Примерами могут служить анализ промывных вод в ваннах отмывки гальванического производства, контроль за приготовлением технологических растворов в производственных условиях и т.п.
Кондуктометрическое титрование
Несомненно, большими аналитическими возможностями обладает кондуктометрическое титрование. Титрование позволяет восполнить недостаток селективности определения применением селективного к анализируемому иону титранта. Известны примеры кислотно-основного, осадительного, комплексонометрического титрований. Точность кондуктометрического титрования составляет 1%, но если принять меры по термостатированию анализируемого раствора, то точность определения можно в несколько раз увеличить.
Точка эквивалентности на графике находится пересечением двух прямых. Одна прямая (до точки эквивалентности) отражает изменение концентрации анализируемого иона и ионов титранта, а другая (после точки эквивалентности) является следствием увеличения концентрации ионов титранта.
Однако не всегда кривая титрования имеет такой вид. На рис. 2 приведены в качестве примера кривые титрования, полученные в результате различных аналитических определений.
Вид кривых очевидно различен. В связи с этим возникает закономерный вопрос о причинах различий и возможности прогнозирования вида кривой на основании данных о свойствах анализируемого иона и вещества титранта. В большинстве случаев прогноз возможен, поскольку вид кривой титрования определяется разностью эквивалентных электропроводностей анализируемого иона и ионов, составляющих вещество титранта.
Рассмотрим несложный расчет, позволяющий прогнозировать вид кривой титрования. Прежде всего, нужно ясно представить себе перечень ионов, принимающих участие в процессе титрования. Пусть нам предстоит определить хлорид с помощью осадительной реакции с нитратом серебра (рис. 2а):
Cl- + Ag+ + NO3- = AgCl + NO3-.
Не вызывает сомнения, что в процессе титрования до точки эквивалентности происходит уменьшение ионов Cl- и NO3- Увеличение концентрации ионов Ag+ практически не происходит, так как серебро осаждается ионом Cl- В связи с этим можно утверждать, что динамика электропроводности происходит со скоростью, пропорциональной сумме
-λ0Cl + λ0NO3 =-0,00655 + 0,00617 = -0,00038 Ом-1 м2 г-экв-1.
Знак '-' перед электропроводностью λ0Cl говорит о том, что концентрация Cl в результате титрования уменьшается. Знак '+' перед λ0NO3 свидетельствует об увеличении концентраци NO3.
Полученное в итоге отрицательное число -0,00038 Ом-1 м2 г-экв-1 указывает на то, что при титрованиии до точки эквивалентности электропроводность раствора уменьшается.
После точки эквивалентности электропроводность будет повышатьcя, так как эту ветвь титрования полностью определяет титрант, т.е. ионы Ag и NO3:
λ0Ag + λ0NO3 = 0,005436 + 0,00617 = 0,011606 Ом-1 м2 г-экв-1.
1.1 Особенности кондуктометрических методов анализа
1. Возможность проводить определение не только в прозрачных, но и в окрашенных и мутных растворах, а также в присутствии окислителей, восстановителей органических веществ.
2. Возможность определения различных неорганических и органических индивидуальных соединений.
3. Высокая чувствительность метода, позволяющая работать с разбавленными растворами.
4. Анализ водных и органических растворов.
5. Возможность автоматизации процесса (хронокондуктометрия).
6. Использование разнообразных типов реакций.
7. Во многих случаях отсутствие необходимости проводить предварительную пробоподготовку.
8. Простота определения конечной точки титрования по пересечению двух прямых.
9. Возможность проведения дифференцированного титрования смесей электролитов, что невозможно при титровании с визуальной индикацией конечной точки титрования.[1–3]
2. Примеры использования кондуктометрии в анализе объектов окружающей среды
Экспресс методы контроля качества сырья, параметров технологических процессов и готовой продукции в сыроделии [4–8]
В сыродельной промышленности, перерабатывающей скоропортящееся сырье, очень важно для организации оперативного контроля его качественных показателей, параметров технологических процессов, а также готовой продукции использование достаточно точных экспресс-методов анализа.
Для оперативного контроля содержания сухих веществ в молочной сыворотке – сырье предлагается ареометрический метод, основанный на измерении ее плотности с помощью ареометра. Необходимость контроля этого показателя продиктована тем, что нормы расхода сыворотки на производство большинства продуктов на ее основе дифференцированы по содержанию сухих веществ.
Прослеживается линейная зависимость плотности молочной сыворотки от содержания сухих веществ. Более высокое содержание сухих веществ в подсырной сыворотке при одинаковом значении показателя плотности обусловлено повышенным в 1,5 раза содержанием минеральных веществ в творожной сыворотке.
Абсолютная погрешность измерения массовой доли сухих веществ предлагаемым методом не превышает 0,1%.
Для организации контроля данного показателя в молочной сыворотке предлагается использовать стандартный набор ареометров, выпускаемый Клинским (Московской области) заводом «Химлаборприбор», обеспечивающий возможность измерения показателя плотности в указанном диапазоне значений с точностью до пятого знака.
Для оперативного контроля массовой доли сухих веществ в молочной сыворотке-сырье, а также в процессе ее концентрирования как методом вакуум_выпаривания, так и методом баромембранного фракционирования наиболее целесообразно использование рефрактометрии.
Рефрактометрия – классический пример оптического экспрессного микрометода, так как измерение показателя преломления осуществляется в течение нескольких минут, а для выполнения измерения достаточно 1–2 капель анализируемого раствора.
Физическая сущность метода состоит в преломлении луча света при переходе из одной среды в другую (одна среда – стеклянная призма, другая – анализируемый раствор).
Каждое вещество, находящееся в растворе в смеси с другими компонентами, сохраняет свою преломляющую способность, поэтому показатель преломления – величина аддитивная. Преломляющие свойства каждого вещества обусловлены строением его молекулы (т.е. природой) и характеризуются молекулярной рефракцией, которая не зависит от агрегатного состояния вещества в растворе.
На основании статистической обработки большого массива экспериментальных данных построены графики зависимости коэффициента преломления молочной сыворотки – сырья и продуктов ее переработки от концентрации сухих веществ. Сравнение указанных графиков показывает, что при адекватном значении показателя преломления содержание сухих веществ в ретентате и сгущенной сыворотке существенно различно. Это обусловлено различной природой доминирующего компонента в анализируемом материале – лактозы в сгущенной сыворотке и белков в ретентате.
Определены границы абсолютной погрешности измерений, которые в диапазоне наиболее часто встречающихся значений концентрации находятся на уровне арбитражного метода (высушивание пробы до постоянного веса).
Для выполнения измерений рекомендуются отечественные портативные рефрактометры марок «Карат-МТ», ИРФ-470, а также лабораторный (стационарный) рефрактометр марки ИРФ-454Б2М.
Очевидно, что стационарный прибор обеспечивает более широкий диапазон измерений коэффициента преломления, более точен (предел допускаемой основной погрешности по показателю преломления в 2,5–3 раза ниже по сравнению с портативным), но более громоздкий, так как имеет значительно большую массу и габариты.
Широкие возможности для оперативного контроля концентрации электролитов в растворах открывает использование метода прямой кондуктометрии.
Сущность метода состоит в том, что электролиты в растворе диссоциируют на ионы, концентрация которых определяет его электропроводимость.
Учитывая линейный характер зависимости удельной электропроводности растворов от концентрации электролитов, нами разработан рекомендуется для практического использования целый ряд экспрессметодов, основанных на данном электрохимическом эффекте.
В связи с тем, что количественное содержание поваренной соли в соленой подсырной сыворотке определяет направления дальнейшего ее использования, изучена зависимость удельной электропроводности подсырной сыворотки от массовой доли хлористого натрия. Очевидно, что широкий диапазон исследованных концентраций хлористого натрия позволяет осуществлять контроль по данному показателю всех видов подсырной сыворотки – сырья от несоленой (т.н. сладкой сыворотки) до соленой сыворотки, получаемой при полной посолке сыра «в зерне», а также в смесях соленой и сладкой сыворотки, получаемых при любом их соотношении. Необходимость контроля таких смесей диктуется повседневной практикой.
На основе кондуктометрии разработана также методика определения массовой доли поваренной соли в сычужном сыре. При этом в качестве анализируемого объекта использовалась водная вытяжка сычужного сыра.
Установлено, что погрешность разработанного метода не превышает арбитражного; преимущества состоят в значительном сокращении времени на выполнение единичного анализа и в отсутствии необходимости использования дорогостоящих реактивов и, в первую очередь, азотнокислого серебра.
Изучена возможность использования данного метода и для оперативного контроля концентрации хлористого натрия в рассоле, используемом для посолки сычужных сыров. Зависимость удельной электропроводности разбавленного в два раза рассола от концентрации хлористого натрия. Наряду с оперативностью контроля данный метод позволяет определять именно концентрацию хлористого натрия в рассоле, а не общего содержания сухих веществ, что имеет место при широко распространенном ареометрическом методе контроля, не учитывающем диффузию в рассол в процессе посолки других компонентов сыра – лактозы и азотистых соединений.
В целях оперативного контроля уровня деминерализации молочной сыворотки в процессе электродиализа при производстве сухой деминерализованной сыворотки изучена зависимость удельной электропроводности сгущенной (30%-ной по содержанию сухих веществ) подсырной сыворотки от содержания минеральных веществ (зольности).
Данная методика включена в технологическую инструкцию по производству деминерализованной сыворотки как оперативный метод контроля основного параметра технологического процесса – зольности сыворотки.
Общий вид и техническая характеристика рекомендуемого для широкого практического применения при освоении указанных выше экспресс-методов портативного кондуктометра немецкой фирмы «HANNA Instruments» модели HI 8733. Прибор высокоточен, надежен и удобен в работе. Время, затрачиваемое на измерение показателя удельной электропроводности исследуемого образца с его помощью, не превышает двух минут при продолжительности определения показателя зольности методом сжигания около 3 часов.
С целью оперативного контроля массовой долилактозы в молочной сыворотке, ее концентратах и молочном сахаре разработан поляриметрический метод, основанный на физическом свойстве (оптической активности углеводов, в том числе и лактозы), проявляющемся в способности вращать плоскость поляризованного света. Учитывая линейную зависимость угла вращения раствора от концентрации лактозы (Λ, %) выведено уравнение, адекватно описывающее значение концентрации лактозы от угла вращения (оS), представленное на рис. 10.
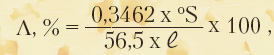
где оS – показания сахариметра (поляриметра, шкала которого проградуирована в градусах сахарозы);
0,3462 – коэффициент пересчета oS в круговые градусы;
56,5 – удельное (правое) вращение лактозы в круговых градусах;
e – длина кюветы (поляриметрической трубки), дм.
Там же представлен общий вид и краткая техническая характеристика сахариметра универсального, т.е. поляриметра, шкала которого проградуирована в градусах сахарозы (оS), модели «СУ-4», серийноизготовляемого Киевским заводом аналитических приборов. Абсолютная погрешность метода не превышает 0,15%, а продолжительность единичного анализа составляет 8! 10 мин при продолжительности широко распространенных химических методов анализа (Бертрана, Шоорля, иодометрического) не менее 2-х часов.
Экспериментально, при достаточно высокойстепени корреляции, установлена зависимость между активной и титруемой кислотностью молочной сыворотки. Она позволяет получить оперативную информацию об уровне как титруемой, так и активной кислотности, измерив только один показатель, что очень удобно в практической работе.
Аналитические возможности жидкостных и ионных хроматографов «ЦветЯуза» в контроле загрязнений окружающей среды
Принцип работы жидкостного хроматографа ЦветЯуза с амперометрическим и кондуктометрическим детекторами [15]
На приборе можно реализовать все основные режимы жидкостной хроматографии: обращеннофазном, ион-парном или ионном и др. Амперометрическое детектирование основано на измерении электрического тока, возникающего при окислении (восстановлении) анализируемого вещества на поверхности рабочего электрода, находящего под определенным потенциалом. В хроматографе «ЦветЯуза» используется ячейка малого объема типа «стенка-струя», время нахождения молекул вещества на поверхности электрода составляет всего лишь миллисекунды, т.е. намного меньше, чем требуется для их полного превращения (окисления, восстановления) на поверхности, поэтому степень превращения составляет всего лишь 5–10%. При этом чувствительность детектора остается всё равно очень высокой из-за малых шумов (10-12 А).
Хроматограф представляет собой моноблок, в котором находятся термостат колонок с диапазоном термостатирования от 30 до 80 0С (в термостате может быть установлено до трёх хроматографических колонок), детектор в термостате (диапазон термостатирования от 30 до 50 0С) и электронный блок. На передней неподвижной панели внизу с правой стороны установлены кран-дозатор с ручным приводом и штуцер для ввода пробы. Насос (типа Марафон-2) создает регулируемый поток элюента, поступающего на его вход из соответствующей емкости для элюента через кран (Rheodyne-7010) в аналитическую колонку и амперометрическую ячейку.
Электрохимическая ячейка представляет собой металлический блок из нержавеющей стали, в который через специальное сопло подается элюент из колонки. На расстоянии 0,4–0,1 мм от сопла расположен рабочий электрод из стеклоуглерода (либо золота, платины или серебра), который должен быть предварительно механически отполирован до зеркальной поверхности. В качестве вспомогательного электрода используется сам корпус ячейки.
Импульсный режим применяется в основном для определения сахаров, аминокислот, спиртов. Поскольку для них характерно быстрое отравление рабочего электрода (Au или Pt), что приводит к сильному увеличению предела обнаружения и ухудшению воспроизводимости получаемых результатов. Адсорбированные продукты реакции могут быть удалены приложением большого положительного потенциала, в результате чего образуется оксид благородного металла. Промежуточный продукт реакции окисления (AuOH и PtOH) реагирует с кислородом из Н2О с образованием конечного соединения. Полученные стабильные оксиды (AuO или PtO) инертны и могут быть удалены приложением на электрод отрицательного потенциала с восстановлением первоначальной реакционной способности чистой поверхности рабочего электрода.
Аналитические возможности ионного хроматографа «ЦветЯуза» с кондуктометрическим детектором [13–15]
Эта модель применяется для анализа анионов и катионов как органических, так и неорганических соединений. В таблице 6 приведён перечень смесей, анализируемых методами ионной хроматографии. В таблице 7 приведены примеры применения ИХ в анализе пищи. Ионная хроматография (ИХ) широко применяется в контроле загрязнений окружающей среды: контроль кислых газов в воздухе и выбросах, анионов в питьевой, поверхностной и сточных водах.
По применениям ИХ вышли обзоры: по контролю загрязнений окружающей среды, по анализу пищевых продуктов.
Очень важно определение бромата ИХ в питьевой озонированной воде, т. к. бромат потенциальный канцероген при 0,05 мкг/л. Утверждена официальная методика определения бромата ИХ (ИСО 15061:2001).
Для оценки экологического состояния морских вод предложена ИХ определения соотношения иодида к иодату.
Приведённые примеры показывают уникальные возможности ЦветЯузы с АД в контроле загрязнений окружающей среды, пищевых продуктов и в клинических анализах.
Таблица 1. Перечень типов рабочих электродов и соединений, определяемых на них
|
Материал рабочего электрода |
Определяемые соединения |
| Стеклоуглерод | Универсальный, но наиболее пригоден для анализа: катехоламинов и их метаболитов, фенолов, хлорфенолов, нафтолов, катехолов, ароматических аминов, нитроароматических соединений, хинонов, полиенов, тиолов, дисульфидов и др. |
| Золото | Алифатические спирты, моносахара, дисахара, олигосахара, алифатические амины, аминоспирты, аминосахара, нитроароматические соединения, аминокислоты, серусодержащие пестициды, этилентиомочевина |
| Платина | Спирты, гликоли, альдегиды, гипохлорит, арсенит, гидразины, ацетилхолин |
| Серебро | Цианид, сульфид, сульфит, тиосульфат, тиоцианат, бромид, иодид, гидросульфид |
| Ртуть | Тиолы, дисульфиды, нитрозамины, восстанавливаемые металлы |
| Медь | Сахара, аминокислоты, пептиды, полипептиды, белки |
| Никель | Сахара, спирты, аминокислоты |
| Палладий | Ароматические углеводороды |
Цитометрия фитопланктона с использованием кондуктометрического цитометра [16]
Здоровье человека непосредственно связано с экологическим состоянием водных экосистем, являющихся важным компонентом окружающей среды. Причем качество водных систем в значительной степени характеризуется параметрами биоты, среди которых биомасса фитопланктона и его таксонометрический состав. Однако существующие методы определения этих параметров не оперативны и трудоёмки. Поэтому актуальной задачей является разработка новых методов и средств изучения состояния водных экосистем, свободных от указанных недостатков. Нами исследована возможность применения кондуктометрического цитометра, позволяющего получить информацию о концентрации и размерах клеток путём регистрации изменения проводимости при прохождении частицы в канале цитометра. В результате проведённых исследований была разработана методика пробоподготовки и цитометрирования фитопланктона, позволяющая проводить таксонометрический анализ клеток. Работоспособность методики подтверждена сравнительным анализом результатов определения количества клеток визуально, при помощи микроскопа и с использованием кондуктометрического цитометра.
3. Современные приборы
Кондуктометр AMI Rescon
Автоматический анализатор для измерения удельного сопротивления / удельной электропроводимости в особо чистой воде.
- Большой ЖК-дисплей с подсветкой для вывода результатов измерений и состояния прибора.
- Рабочий диапазон: 0.005–1000 мкСм/см (0.01 – 100 Мом-см соответственно). – Температурная компенсация
- Сигнализация нарушения допустимого температурного диапазона, граничных параметров величины потока пробы.
- 2 сигнальных выхода 0/4 – 20 мА.
- Анализатор поставляется в комплекте, на монтажной панели, полностью готовым к работе.
Технические данные:
Расход пробы: 70 – 90 л/ч
Макс. давление: 2 бар
Макс. температура: 50 °С
Рабочий диапазон: от 0,005 до 1000 мкСм/см
Точность: от 0,01 до 20 Мом-см ± 0.5%
0.05 дo 20 мкСм/см: ± 0.5%
Кондуктометр FAM Powercon Acid
Автоматический анализатор для измерения электропроводимости пробы после Н-катионитного фильтра. Используется для контроля качества воды, пара и конденсата.
Электропроводность пробы после Н-катионитного фильтра – Большой жидкокристаллический дисплей с подсветкой для вывода результатов измерений и состояния прибора. – Диапазон измерения, от 0,055 мкСм/см до 1 мСм/см. – Несколько вариантов термокомпенсации. – Сигнализация при слишком высокой или слишком низкой температуре пробы. – Два выходных токовых сигнала 0/4 – 20 мА, гальванически развязанные от цепей датчика, для электропроводимостии/или температуры. – Дискретный выход типа «сухой контакт» для обобщенной сигнализации о неисправности прибора. – Два выходных реле типа «сухой контакт», срабатывающие по заданным пределам. – Один дискретный вход для «сухого» контакта с программируемыми функциями. В поставку включается. – Вторичный прибор FAM Powercon в алюминиевом корпусе {IР65} – Проточная ячейка Catcon для одного датчика электропроводности со встроенным катионитным фильтром – Датчик расхода пробы – Датчик электропроводности.
Кондуктометр FAM Powercon Specific
Автоматический анализатор для измерения общей удельной электропроводимости пробы. Используется в различных областях, где необходимо контролировать электропроводимость в достаточно широком диапазоне.
Общая удельная электропроводность питательной воды, пара и конденсата.
– Большой жидкокристаллический дисплей с подсветкой для вывода результатов измерений и состояния прибора.
– Диапазон измерения: от 0,055 мкСм/см до 1 мСм/см.
- Несколько вариантов термокомпенсации.
– Сигнализация при слишком высокой или слишком низкой температуре пробы.
- Два выходных токовых сигнала 0/4 – 20 мА, гальванически развязанные от цепей датчика, для электропроводимости и / или температуры.
- Дискретный выход типа «сухой контакт' для обобщенной сигнализации о неисправности прибора.
– Два выходных реле типа «сухой контакт», срабатывающие по заданным пределам.
- Один дискретный вход для «сухого» контакта с программируемыми функциями.
Дополнительные принадлежности:
– Интерфейс RS485 с поддержкой протоколов PROFIBUS DP/SWANBUS или MODBUS ASCII/MODBUS RTU
Кондуктометр FAM Powercon +
Электропроводность пробы до и после Н-катионитного фильтра.
- Большой жидкокристаллический дисплей с подсветкой для вывода результатов измерений и состояния прибора.
– Диапазон измерения, от 0,055 мкСм/см до 1 мСм/см.
- Несколько вариантов термокомпенсации.
– Сигнализация при слишком высокой или слишком низкой температуре пробы.
- Два выходных токовых сигнала 0/4 – 20 мА, гальванически развязанные от цепей датчика, для электропроводности до/после Н-катионитного фильтра и / или температуры.
– Дискретный выход типа «сухой контакт» для обобщенной сигнализации о неисправности прибора.
– Два выходных реле типа «сухой контакт», срабатывающие при нарушении заданных параметров.
– Один дискретный вход для «сухого» контакта с программируемыми функциями.
В поставку включается:
– Вторичный прибор FAM Powercon+ на алюминиевом корпусе.
- Проточная ячейка для двух датчиков электропроводности со встроенным катионитным фильтром- 2 датчика электропроводности.
Монитор AMI Deltacon DG
Полностью смонтированная система на панели из нержавеющей стали:
– Трансмиттер AMI Deltacon DG в алюминиевом корпусе (IP 66)
– Swansensors UP-Con1000-SL Три двухэлектродных датчика УЭП со встроенными температурными датчиками Pt1000.
– Проточная ячейка Catcon-Plus-SL с вентилем регулировки расхода пробы, цифровым расходомером пробы и встроенным H-фильтром
– Блок дегазации пробы с холодильником и нагревателем пробы из нержавеющей стали.
– Контроллер DG для контроля дегазации пробы с датчиком давления (IP 66)
– Заводское тестирование, полная готовность для монтажа и эксплуатации.
Спецификация:
- Диапазон измерения УЭП: 0.055 до 1000 мкСм/см.
– Рачет pH в диапазоне от pH 7.5 до 10.5 (VGB-directive 450L)
- Оасчет концентрации аммиака в диапазоне от 0.01 до 10 мг/л (ppm)
- Одновременное отображение на дисплее всех значений УЭП, pH и концентрации аммиака, а также температуры и расхода пробы.
– Два токовых выхода (0/4 – 20 мA) для измеренных значений.[17]
Литература
1. Харитонов Ю.Я. Аналитическая химия. Кн. 2. – М.: Высшая школа. 2003. – 345 с.
1. Брайнина Х.З., Нейман Е.Я., Слепушкин В.В. Инверсионные электроаналитические методы. – М.: Химия, 1988. – 239 с.
2. Электрохимические методы в контроле окружающей среды. – М.: Химия, 1990. – 238 с.
3. Сурова Н.А. Использование вольтамперометрической компьютеризированной системы для анализа экологических объектов // Ученые записки Симферопольского государственного университета. Математика, физика, химия. – 1997. – №4 (43). – С. 112–119.
4. Гейровский Я., Кута Я. Основы полярографии. – М.: Мир, 1965. – 295 с.
5. Ройзенблат Е.М., Веретина Г.И. О чувствительности определения ртути методом инверсионной вольтампереметрии на графитовом электроде // Журн. аналит. химии. – 1974. – Т. 29, №12. – С. 2376–2380.
6. Будников Г.К. Определение следовых количеств веществ как проблема современной аналитической химии // Соросовский Образовательный Журнал. 2000. Т. 6, №3. С. 45–51.
7. Эйхлер В. Яды в нашей пище. М.: Мир, 1993. – 189 с.
8. Золотов Ю.А., Кимстач В.А., Кузьмин Н.М. и др. // Рос. хим. журн. 1993. Т. 37, №4. С. 20–27.
9. Майстренко В.Н., Хамитов Р.З., Будников Г.К. Эколого-аналитический мониторинг супертоксикантов. М.: Химия, 1996. – 319 с.
10. Будников Г.К. Диоксины и родственные соединения как экотоксиканты // Соросовский Образовательный Журнал. 1997. №8. С. 38–44.
11. Пурмаль А.П. Антропогенная токсикация планеты // Там же. №9. С. 39–51.
12. Некоторые вопросы токсичности ионов металлов / Под ред. Х. Зигеля, А. Зигель. М.: Мир, 1993. 368 с.
13. Шведене Н.В. Ионоселективные электроды // Соросовский Образовательный Журнал. 1999. №5. С. 60–65.
14. А.Я. Яшин, Я.И. Яшин Аналитические возможности жидкостных и ионных хроматографов «ЦветЯуза» в контроле загрязнений окружающей среды
15. Козлов А.В. Цитометрия фитопланктона с использованием кондуктометрического цитометра